Специфичность фермента амилазы
Изопентенилпирофосфат-изомераза содержит содержит свободные сульфгидридные группы, верятно, в виде радикала цис в белковой молекуле, и именно благодаря им обеспечивается указанная выше реакция, имеющая огромное значение для синтеза полизиопреноидов и стеролов.
Лигазы (синтетазы).
К лигазам относятся ферменты, катализирующие соединение друг с другом молекул, сопряженное с гидролизом пиро
фосфатной связи в молекуле АТФ или иного нуклеозидтрифосфата.
В качестве примера действия лигазы можно привести синтез пантотеновой кислоты из
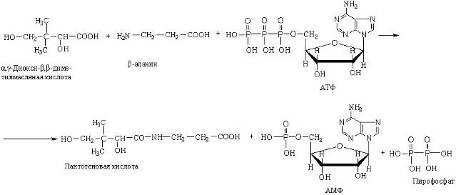
1.2 АМИЛАЗЫ. СТРОЕНИЕ, ФУНКЦИИ
Амилазы (от лат. amylum - крахмал), ферменты класса гидролаз, катализирующие гидролиз крахмала, гликогена и др. родственных олиго- и полисахаридов, гл. обр. по 1,4![]() глюкозидной связи (см., напр., схему в ст. О-Гликозидгидролазы). При приготовлении дрожжевого теста дрожжи разлагают крахмал с помощью амилазы до ди- и трисахаридов, которые потом используются в жизнедеятельности, образуя в результате спирт, углекислый газ (CO2) и другие метаболиты, которые придают хлебу специфический вкус и «поднимают» тесто. Однако, это длительный процесс, поэтому в современных технологиях амилаза используется как одно из важных составляющих специальной добавки, ускоряющий процесс брожения. Бактериальная амилаза используется в стиральных порошках для разложения крахмала, присутствующего в белье.
глюкозидной связи (см., напр., схему в ст. О-Гликозидгидролазы). При приготовлении дрожжевого теста дрожжи разлагают крахмал с помощью амилазы до ди- и трисахаридов, которые потом используются в жизнедеятельности, образуя в результате спирт, углекислый газ (CO2) и другие метаболиты, которые придают хлебу специфический вкус и «поднимают» тесто. Однако, это длительный процесс, поэтому в современных технологиях амилаза используется как одно из важных составляющих специальной добавки, ускоряющий процесс брожения. Бактериальная амилаза используется в стиральных порошках для разложения крахмала, присутствующего в белье.
![]() А. (мол. м. 50 тыс.) участвует в гидролизе сахаров, содержащих подряд три или более остатков глюкозы. Расщепление связей может происходить между любыми остатками глюкозы, причем остатки моносахаридов в месте разрыва имеют конфигурацию
А. (мол. м. 50 тыс.) участвует в гидролизе сахаров, содержащих подряд три или более остатков глюкозы. Расщепление связей может происходить между любыми остатками глюкозы, причем остатки моносахаридов в месте разрыва имеют конфигурацию![]() аномеров.
аномеров.![]() А. превращает амилозу крахмала в глюкозу и мальтозу. Находящийся в крахмале амилопектин, содержащий в молекуле 1,6
А. превращает амилозу крахмала в глюкозу и мальтозу. Находящийся в крахмале амилопектин, содержащий в молекуле 1,6![]() связи, полностью не гидролизуется - остается разветвленный полисахарид, т. наз. "остаточный декстрин".
связи, полностью не гидролизуется - остается разветвленный полисахарид, т. наз. "остаточный декстрин".![]() А. обладает слабокислыми св-вами. Ионы Са2+ и Cl- активируют ее. Присутствует во всех тканях животных и растений, а также в микроорганизмах. По каталитич. активности ферменты из разных источников значительно отличаются друг от друга.
А. обладает слабокислыми св-вами. Ионы Са2+ и Cl- активируют ее. Присутствует во всех тканях животных и растений, а также в микроорганизмах. По каталитич. активности ферменты из разных источников значительно отличаются друг от друга.![]() А. слюны, поджелудочной железы и слизистой кишечника участвуют в переваривании пищи,
А. слюны, поджелудочной железы и слизистой кишечника участвуют в переваривании пищи,![]() А. печени расщепляет гликоген.
А. печени расщепляет гликоген.
![]() А. (мол. м. 50-200 тыс.) последовательно отщепляет остатки
А. (мол. м. 50-200 тыс.) последовательно отщепляет остатки![]() мальтозы от невосстанавливающего конца цепи полисахаридов. Под действием
мальтозы от невосстанавливающего конца цепи полисахаридов. Под действием![]() А. из амилозы образуется мальтоза, а из амилопектина также "остаточный декстрин". Содержится
А. из амилозы образуется мальтоза, а из амилопектина также "остаточный декстрин". Содержится![]() А. в солоде.
А. в солоде.
![]() А. (экзо-1,4
А. (экзо-1,4![]() глюкозидаза; мол. м. 50-100 тыс.) последовательно отщепляет концевые остатки
глюкозидаза; мол. м. 50-100 тыс.) последовательно отщепляет концевые остатки![]() D-глюкозы от невосстанавливающих концов цепей полисахаридов с образованием
D-глюкозы от невосстанавливающих концов цепей полисахаридов с образованием![]() D-глюкозы. Способна также расщеплять 1,6
D-глюкозы. Способна также расщеплять 1,6![]() связь, если следующие за ней моносахариды соединены в положениях 1 и 4. Содержится в плесневых грибах. Определение активности А. используют в диагностич. целях, в частности для идентификации гликогеноза. А. (в т. ч. иммобилизованные) применяют в пром-сти:
связь, если следующие за ней моносахариды соединены в положениях 1 и 4. Содержится в плесневых грибах. Определение активности А. используют в диагностич. целях, в частности для идентификации гликогеноза. А. (в т. ч. иммобилизованные) применяют в пром-сти:![]() А.-для "осахаривания" крахмала,
А.-для "осахаривания" крахмала,![]() А.-для произ-ва глюкозы.
А.-для произ-ва глюкозы.
Функции. Амилаза - гидролитический фермент - разлагает крахмал и гликоген до мальтозы. Амилаза образуется преимущественно в слюнных железах и поджелудочной железе, поступает затем соответственно в полость рта или просвет двенадцатиперстной кишки и участвует в переваривании углеводов пищи. В сыворотке крови выделяют соответственно панкреатический и слюнной изоферменты амилазы. Значительно более низкой амилазной активностью обладают также такие органы как яичники, фаллопиевы трубы, тонкий и толстый кишечник и печень. Фермент выводится почками. Следовательно, увеличение сывороточной активности амилазы приводит к повышению активности амилазы в моче. Амилаза может образовывать крупные по размеру комплексы с иммуноглобулинами и другими белками плазмы, поэтому не проходит через почечные клубочки, поэтому содержание ее в сыворотке возрастает, в моче наблюдается нормальная активность амилазы.
Слюна содержит значительное количество амилазы — фермента, принимающего участие в переваривании углеводов, а также ферменты, расщепляющие белки. Все они активны только при щелочной или нейтральной реакции среды. Поэтому кислый желудочный сок прекращает их действие. Но, тем не менее, их влияние продолжается некоторое время в желудке, потому что пищевой комок не сразу пропитывается желудочным соком.
Слюна обладает бактерицидными (убивающими микробы) свойствами. Она предупреждает развитие кариеса зубов благодаря присутствию в ней фермента лизоцима. У человека слюноотделение связано и с речевой функцией: слюна обеспечивает во время речи увлажнение слизистой оболочки ротовой полости (установлено, что слюноотделение сопровождает даже акт письма). В течение суток выделяется от 0,5 л до 2 л слюны.
1.3 СПЕЦИФИЧНОСТЬ АМИЛАЗЫ Ферменты обладают очень высокой специфичностью. Эта специфичность обусловлена особой формой молекулы фермента, точно соответствующей форме молекулы субстрата. Эту гипотезу называют гипотезой “ключа и замка”: субстрат сравнивается в ней с ключом, который точно подходит к замку, т.е. к ферменту. Далее на основании этой гипотезы уже в 1959 году новую интерпретацию гипотезы “ключа и замка” предложил Кошланд. Он делает вывод о гибкости активных центров ферментов. Согласно этому предположению, субстрат соединяясь с ферментом, вызывает изменения в структуре последнего. Подходящей аналогией в этом случае может служить перчатка, которая при надевании на руку соответствующим образом изменяет свою форму.Амилазы различного происхождения имеют много общих свойств: хорошо растворяются в воде или в сильно разбавленных растворах солей. Более концентрированные растворы солей (например 20-30% - ные растворы сульфата аммония) вызывают осаждение этих ферментов. Амилаза легко растворяются в разбавленных растворах этилового спирта, но осаждаются при его концентрации в среде свыше 60%. Белок амилаз обладает слабокислыми свойствами; изоэлектрическая точка ферментов колеблется в пределах рН 4,2 - 5,7. Молекулярная масса солодовой амилазы 60000, амилаз микроскопических грибов - 45000-50000. Многие из амилазы получены либо в высокоочищенном, либо в кристаллическом виде. Ионы кальция оказывают стабилизирующее действие на амилазу. Это впервые было обнаружено Воллерштейном, затем подтверждено Накамурой. В настоящее время это явление отмечено почти для всех амилаз. Однако теоретически этот вопрос применительно к промышленному гидролизу крахмала до сих пор не разработан.Гидролиз крахмала амилазами:
Другие рефераты на тему «Химия»:
- Синтез и свойства комплексов рения (IV) с некоторыми аминокислотами
- Исследование механизма синергического действия смесей цинковых солей органических кислот и полиолов при термическом распаде поливинилхлорида (ПВХ)
- Частицы и коллектив. Неразличимость и симметрия Коррекция статистических сумм для трансляции и ротации
- История открытия элементов
- Роль Менеделеева в развитии мировой науки
