Коллоидная химия
Вязкость растворов, содержащих макромолекулы, обычно выше вязкости растворов НМС и коллоидных растворов тех же концентраций.
Отклонения вязкости растворов ВМС от законов, которым подчиняются растворы НМС, следует объяснить особенностями гидродинамики систем, содержащих вытянутые и гибкие макромолекулы и наличием в них ассоциатов и легко разрушаемых структур.
6. Определение молекулярной
массы по вязкости их растворов
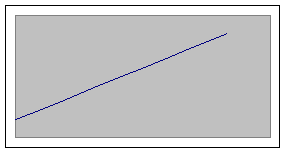
Приведенная вязкость растворов одного и того же полимера обычно возрастает с повышением концентрации, причем это возрастание в интервале небольших концентраций происходит по прямой.
Отрезок, отсекаемый этой прямой отвечает величине характеристической вязкости ![]() , отражающей гидродинамическое сопротивление потоку молекул данного полимера. Характеристическая вязкость представляет собой приведенную вязкость при бесконечно большом разбавлении раствора.
, отражающей гидродинамическое сопротивление потоку молекул данного полимера. Характеристическая вязкость представляет собой приведенную вязкость при бесконечно большом разбавлении раствора.
В настоящее время для определения молекулярного веса предложено уравнение, учитывающее взаимодействие макромолекул даже в разбавленных растворах и изменение константы ![]() с длиной молекулы:
с длиной молекулы:
![]() ,
,
где ![]() - коэффициент постоянный для растворов полимергомологического ряда в данном растворителе;
- коэффициент постоянный для растворов полимергомологического ряда в данном растворителе;
![]() - величина, характеризующая форму макромолекул в растворе и связанная с гибкостью цепи.
- величина, характеризующая форму макромолекул в растворе и связанная с гибкостью цепи.
7. Полиэлектролиты и их свойства
Полиэлектролиты – это ВМС, молекулы которых содержат гомогенные группы и в растворах способны распадаться на ионы. По природе содержащихся в них ионогенных групп можно разделить на три категории:
1. полиэлектролиты, содержащие кислотную группу ![]() . Первую группу содержат гуммиарабик, альгинаты, растворимый крахмал, а вторую – агар.
. Первую группу содержат гуммиарабик, альгинаты, растворимый крахмал, а вторую – агар.
2. полиэлектролиты, содержащие основную группу ![]() . Такие вещества в природе не встречаются, но могут быть синтезированы.
. Такие вещества в природе не встречаются, но могут быть синтезированы.
3. полиэлектролиты, содержащие одновременно как кислотную, так и основную группу (полиамфолиты). К ним относятся белки, синтетические полиамфолиты – сополимеры акриловой кислоты и винилпиридина, глютаминовой кислоты и лизина.
Полиэлектролиты, за исключением белков, характеризуются высокой плотностью расположения ионогенных групп – обычно на одно звено цепи приходится по одной ионогенной группе. Вследствие этого молекулы полиэлектролитов могут испытывать в растворе значительные электростатические взаимодействия, что приводит к значительной деформации цепей гибких молекул.
Все высокомолекулярные электролиты растворяются в полярных растворителях, т.к. макромолекулы с гомогенными группами взаимодействуют с полярными жидкостями сильнее, чем с неполярными.
Молекулы белков являются амфотерными соединениями, pH белков ниже 7, т.к. они являются более сильной кислотой, чем основанием.
8. Латексы и дисперсии полимеров. Их применение
Натуральные латексы представляют собой млечный сок бразильской гевеи, синтетические латексы получают путем полимеризации в водной среде непредельных углеводородов – бутадиена, хлоропрена и других мономеров.
Латексы содержат макроскопические и ультра микроскопические частицы, приближающиеся по формуле к сферическим, на поверхности которых адсорбированы стабилизатор – соединения типа белков для натурального латекса и мыла али другие ПАВ у синтетических латексов. Вещество дисперсной фазы состоит из каучука, макромолекулы которого представляют собой гибкие углеводородные цепи, не содержащие или содержащие полярные группы.
Коллоидные системы с твердой дисперсионной средой называют твердые золи. Их можно разделить на системы с газовой, жидкой и твердой дисперсной фазой.
Системы с твердой дисперсионной средой и газовой дисперсной фазой часто называют твердыми пенами.
Системы с твердой дисперсионной средой и жидкой дисперсной фазой можно считать твердыми эмульсиями.
Наибольшее значение имеют системы твердой дисперсионной средой и твердой дисперсной фазой. Натуральные и синтетические латексы широко применяются для получения эластичных пленок, для изготовления эластичных пористых материалов, заменителей кожи, для пропитки корда в шинной промышленности и др.
V. Раздел «Представители гетерогенно – дисперсных систем»
1. Суспензии. Способы получения и стабилизации. Особенности суспензий и их применение
Суспензии – системы с твердой дисперсной фазой и жидкой дисперсионной средой, размеры частиц которых превышают коллоидные размеры.
Методы получения суспензий делят на физико-механические и физико-химические.
К физико-механическим относятся дробление и измельчение твердых материалов, и распыление жидких сред, т.е. диспергирование. В ходе осуществления этого метода химический состав материала не меняется. При физико-химических методах получения суспензий изменяется химический состав материала. К таким методам относятся восстановление оксидов и других металлов, электролиз водных растворов и расплавов солей и др.
Суспензии одновременно поглощают и рассеивают свет, при этом в отличие от опалесцирующих золей суспензии проявляют мутность не только при боковом освещении, но и в проходящем свете. Суспензии, так же как и золи, способны проявлять двойное лучепреломление в потоке.
Поскольку частицы суспензий обладают сравнительно большими размерами, суспензии седиментационно неустойчивы, если плотность дисперсной фазы не очень близка к плотности дисперсной среды и вязкость этой среды не очень велика.
Для суспензий характерен ряд процессов, не свойственных коллоидным системам или протекающих у последних иначе, чем у суспензии. К таким процессам относятся седиментация, флотация, фильтрация и кольматация.
К суспензиям при достаточном содержании влаги относятся почвы и грунты, цементные и известковые растворы, применяемые в строительстве. Суспензиями являются взвеси пигментов в органических средах, применяющихся в качестве масляных красок и цветных лаков, взвеси графита и угля, используемые для создания центров кристаллизации с целью предотвращения образования накипи в котлах и т.д.
2. Эмульсии. Способы получения и стабилизации. Прямые и обратные эмульсии, обращение фаз в эмульсиях, эмульгаторы и деэмульгаторы. Применение эмульсии
Эмульсии – это дисперсные системы, образованные двумя взаимно нерастворимыми жидкостями. Их получают как конденсационными, так и диспергационными методами.
Отличительной особенностью не слишком концентрированных эмульсий является сферическая форма частиц.
Существуют лиофобные и лиофольные – критические эмульсии.
Критические эмульсии – это системы, образующиеся из двух ограниченно смешивающихся жидкостей при температурах, близких к критической температуре смешения, когда поверхностное натяжение на границе фаз становится весьма малым и тепловое движение молекул уже достаточно для диспергирования одной жидкости в другой.
